Kolloidwissen einfach erklärt
Wer sich mit Kolloidherstellung beschäftigt, stößt schnell auf viele technische Begriffe.
Damit Sie die wichtigsten Zusammenhänge rund um Kolloide, Partikel, Stabilität, Ionen, Hochvolt- und Niedervolt-Verfahren leichter verstehen, haben wir die zentralen Fachbegriffe in diesem Glossar einfach und verständlich für Sie erklärt.
Besonders häufig gesucht:
Agglomeration, Brownsche Molekularbewegung, Tyndall-Effekt, Zeta-Potential, Ionen, Kolloid, Elektrolyse, Plasma, Sedimentation, Stabilität.
Schnell zum Begriff:
A · B · C · D · E · F · G · H · I · K · L · N · O · P · Q · R · S · T · U · V · Z
Glossar Kolloidherstellung – alphabetisch
A
Adsorption
Anlagerung von Atomen, Ionen oder Molekülen an der Oberfläche eines Partikels. Bei Kolloiden kann Adsorption die Oberflächenladung, Stabilität und Reaktivität beeinflussen.
Agglomeration
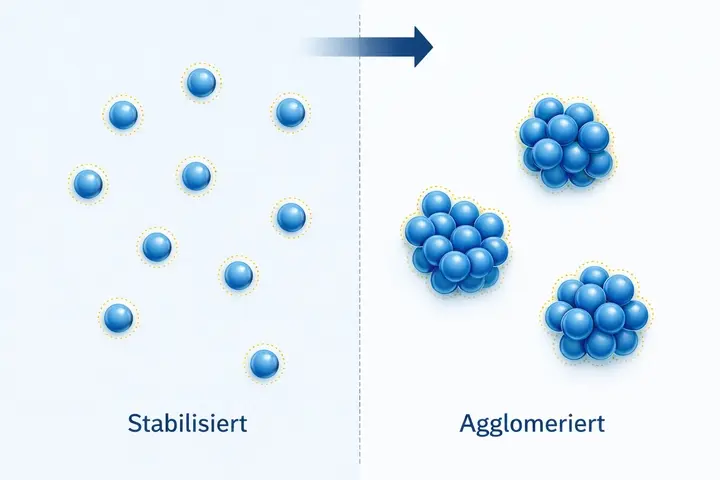
Zusammenballung kleiner Teilchen zu größeren, meist locker verbundenen Verbänden. Agglomeration ist bei Kolloiden meist unerwünscht, weil die feine Verteilung und Stabilität darunter leiden kann.
Aggregation
Zusammenlagerung mehrerer Teilchen zu größeren Einheiten. Der Begriff wird oft ähnlich wie Agglomeration verwendet, kann aber auch eine festere und dauerhaftere Verbindung meinen.
Anionen
Negativ geladene Ionen. Sie können mit Metallionen reagieren und dadurch die Zusammensetzung eines Systems beeinflussen.
Anode
Die Elektrode, an der Oxidation stattfindet. Bei elektrochemischen Vorgängen kann hier Metall aus der Elektrode in Lösung übergehen.
B
Brownsche Molekularbewegung
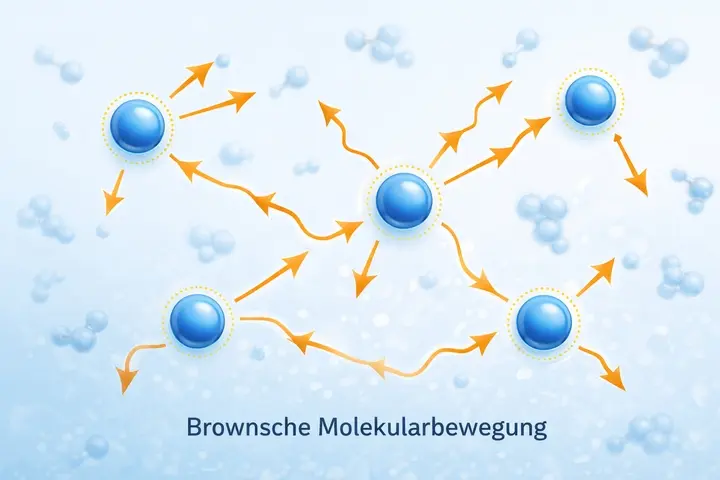
Die ständige, zufällige Bewegung kleinster Teilchen in einer Flüssigkeit. Sie entsteht durch Zusammenstöße mit den Molekülen des umgebenden Mediums und trägt dazu bei, dass sehr kleine Kolloidteilchen in Schwebe bleiben.
C
Charge
Eine einzelne Produktionsmenge. Der Begriff ist wichtig, wenn es um Reproduzierbarkeit, Vergleichbarkeit und Qualitätskontrolle geht.
Cluster
Sehr kleine Ansammlungen weniger Atome oder Moleküle. Sie können als Vorstufe späterer Partikelbildung auftreten.
Contamination / Kontamination
Verunreinigung durch unerwünschte Stoffe, Partikel oder Ionen. Sie kann Reinheit, Stabilität und Qualität eines Kolloids beeinträchtigen.
D
Dispergierung
Feines Verteilen eines Stoffes in einem anderen Medium. Das ist ein zentraler Vorgang bei der Herstellung kolloidaler Systeme.
Disperse Phase
Die fein verteilten Teilchen selbst. Bei Metallkolloiden sind das die Metallpartikel.
Dispersionsmedium
Die Flüssigkeit oder Phase, in der die feinen Teilchen verteilt sind. Bei vielen Kolloiden ist das Wasser.
Dispersion
Ein System, in dem feine Teilchen in einem anderen Medium verteilt sind, ohne vollständig gelöst zu sein.
E
Echte Lösung
Eine Lösung, in der ein Stoff auf molekularer oder ionischer Ebene vollständig gelöst vorliegt. Im Unterschied dazu enthält ein Kolloid fein verteilte Teilchen.
Elektroden
Leitende Bauteile, über die Strom in ein System eingebracht wird. Bei der Kolloidherstellung bestehen sie oft aus dem Metall, das in das System eingebracht werden soll.
Elektrodenabtrag
Materialverlust an der Elektrode durch elektrische, elektrochemische oder physikalische Prozesse. Dieser Vorgang spielt bei vielen Herstellungsverfahren eine zentrale Rolle.
Elektrolyt
Ein Stoff oder eine Lösung, die elektrische Ladung durch bewegliche Ionen transportieren kann.
Elektrolyse
Chemische Umwandlung durch elektrischen Strom. Bei bestimmten Verfahren entstehen dabei Metallionen.
Elektrostatische Abstoßung
Abstoßung zwischen gleich geladenen Teilchen. Sie trägt wesentlich zur Stabilität eines Kolloids bei.
Elementares Metall
Metall in neutraler, nicht ionischer Form. Bei echten Metallkolloiden spricht man häufig von fein verteiltem elementarem Metall.
Erosion
Abtragung von Material durch physikalische oder elektrische Einwirkung, zum Beispiel an Elektroden.
F
Filtration
Abtrennung größerer Partikel oder Verunreinigungen durch einen Filter.
Flokkulation
Bildung lockerer, flockiger Teilchenverbände. Sie kann ein Zeichen nachlassender Stabilität sein.
Funkenentladung
Kurzzeitige elektrische Entladung zwischen Elektroden. Je nach Verfahren kann sie Material aus der Elektrodenoberfläche lösen.
G
Grenzfläche
Übergangsbereich zwischen Partikeloberfläche und umgebender Flüssigkeit. Viele wichtige physikalische und chemische Prozesse laufen genau dort ab.
H
Homogenität
Gleichmäßige Verteilung der Teilchen in der Flüssigkeit. Ein homogenes Kolloid wirkt gleichmäßig und stabil.
Hochvolt-Verfahren
Verfahren, bei denen mit höherer elektrischer Spannung gearbeitet wird. Je nach Technik kann das die Bildung sehr feiner Partikel begünstigen.
Hydroxid
Chemische Verbindung, die unter bestimmten Bedingungen aus Metallionen entstehen kann. Solche Nebenprodukte können die Reinheit beeinflussen.
I
Ionen
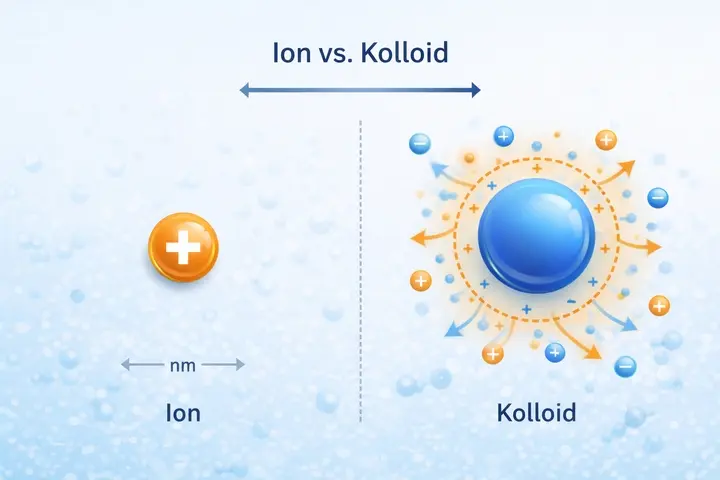
Elektrisch geladene Atome oder Moleküle. Sie sind nicht dasselbe wie elementare kolloidale Partikel.
Ionische Stärke
Maß für die Konzentration gelöster Ionen in einer Flüssigkeit. Eine hohe ionische Stärke kann die Stabilität eines Kolloids beeinflussen.
K
Kathode
Die Elektrode, an der Reduktion stattfindet.
Keimbildung
Beginn der Teilchenentstehung. Dabei bilden sich erste stabile, sehr kleine Einheiten, aus denen später Partikel wachsen können.
Koagulation
Zusammenlagerung von Teilchen zu größeren Einheiten. Dadurch verliert das Kolloid an Stabilität.
Kolloid
Ein fein verteiltes System, bei dem kleine Teilchen in einem anderen Medium verteilt sind, ohne sich vollständig zu lösen.
Kolloidale Dispersion
Eine Dispersion mit sehr feinen Teilchen im kolloidalen Größenbereich.
Komplexbildung
Bindung von Metallionen an andere Moleküle oder Ionen. Dadurch ändert sich ihr chemisches Verhalten.
Konzentration
Menge der enthaltenen Partikel oder Stoffe pro Volumen, zum Beispiel in ppm oder mg/L.
Kontamination
Siehe Verunreinigung.
L
Lagerstabilität
Beschreibt, wie gut ein Kolloid seine Eigenschaften über längere Zeit behält.
Leitfähigkeit
Maß dafür, wie gut eine Flüssigkeit elektrischen Strom leitet. Sie hängt stark vom Ionengehalt ab.
Lichtbogen
Sichtbare elektrische Entladung zwischen zwei Elektroden. Je nach Verfahren kann sie Materialübergänge unterstützen.
N
Nanopartikel
Sehr kleine Teilchen im Nanometerbereich. Viele Kolloide enthalten Partikel in dieser Größenordnung.
Niedervolt-Verfahren
Verfahren mit vergleichsweise niedriger Spannung. Häufig ist die Ionenbildung dabei stärker ausgeprägt als bei energieintensiveren Verfahren.
Nukleation
Fachbegriff für Keimbildung, also den Anfang der Partikelentstehung.
O
Oberflächenenergie
Energiezustand an der Oberfläche eines Partikels. Kleine Partikel besitzen im Verhältnis zu ihrer Masse eine besonders große Oberfläche.
Oberflächenladung
Elektrische Ladung an der Partikeloberfläche. Sie beeinflusst die Stabilität und das Verhalten der Teilchen in der Flüssigkeit.
Oxid
Verbindung eines Metalls mit Sauerstoff. Oxide oder Oxidschichten können Herstellungsprozesse beeinflussen.
Oxidation
Abgabe von Elektronen durch ein Atom, Ion oder Metall. Bei elektrochemischen Prozessen ist sie ein zentraler Vorgang.
P
Partikelgröße
Die Größe der einzelnen Teilchen. Sie beeinflusst Stabilität, Lichtverhalten und optischen Eindruck des Kolloids.
Partikelgrößenverteilung
Beschreibt, ob die Teilchen eher gleich groß oder unterschiedlich groß sind.
Partikelwachstum
Anlagerung weiterer Atome oder kleiner Einheiten an bestehende Partikel.
Peptisation
Wiederzerteilung zusammengeballter Teilchen in ein kolloidales System.
pH-Wert
Maß für den sauren oder basischen Charakter einer Lösung. Er kann die Stabilität und Reaktionsbereitschaft eines Systems beeinflussen.
Plasma
Ein energiereicher Zustand mit freien Ladungsträgern wie Elektronen und Ionen. In bestimmten Verfahren wird Plasma gezielt genutzt.
Plasmaentladung
Elektrische Entladung, bei der Plasma entsteht. Sie kann sehr hohe Energie in das System einbringen.
Plasmonenresonanz
Optischer Effekt, der bei Metallnanopartikeln auftreten kann und die Farbe eines Kolloids mitbestimmt.
ppm
Abkürzung für „parts per million“. Eine häufige Einheit zur Angabe sehr kleiner Konzentrationen.
Q
Qualitätskontrolle
Prüfung von Eigenschaften wie Reinheit, Konzentration, Stabilität oder Leitfähigkeit, um eine gleichbleibende Produktqualität sicherzustellen.
R
Redispersion
Erneutes feines Verteilen von Partikeln nach einer Ablagerung oder Zusammenballung.
Redoxreaktion
Gekoppelter Ablauf von Oxidation und Reduktion.
Reduktion
Aufnahme von Elektronen. Sie ist das Gegenstück zur Oxidation.
Reinheit
Grad, in dem ein System frei von Fremdstoffen, Nebenprodukten oder unerwünschten Ionen ist.
Reinwasser
Besonders ionenarmes Wasser, zum Beispiel destilliertes oder deionisiertes Wasser. Es ist bei der Kolloidherstellung oft wichtig, um Fremdeinflüsse gering zu halten.
S
Sedimentation
Absetzen von Teilchen unter Einfluss der Schwerkraft. Je größer oder schwerer die Teilchen, desto eher kann Sedimentation auftreten.
Spezifische Oberfläche
Oberfläche eines Stoffes im Verhältnis zu seiner Masse oder seinem Volumen. Kleine Partikel haben eine besonders große spezifische Oberfläche.
Stabilität
Beschreibt, wie gut Teilchen über längere Zeit fein verteilt bleiben, ohne sich zusammenzulagern oder abzusetzen.
Suspension
Gemisch aus Flüssigkeit und größeren, ungelösten Feststoffteilchen. Eine Suspension ist gröber als ein Kolloid.
T
Tyndall-Effekt

Streuung von Licht an kolloidalen Teilchen. Dadurch kann ein Lichtstrahl in einer kolloidalen Dispersion sichtbar werden.
U
Ultraschall-Dispergierung
Zerteilung oder Wiederverteilung von Partikeln mit Hilfe von Ultraschall.
V
Van-der-Waals-Kräfte
Schwache Anziehungskräfte zwischen Teilchen. Sie können die Zusammenlagerung von Partikeln begünstigen.
Verunreinigung
Eintrag unerwünschter Stoffe, Ionen oder Partikel in das System.
Z
Zeta-Potential
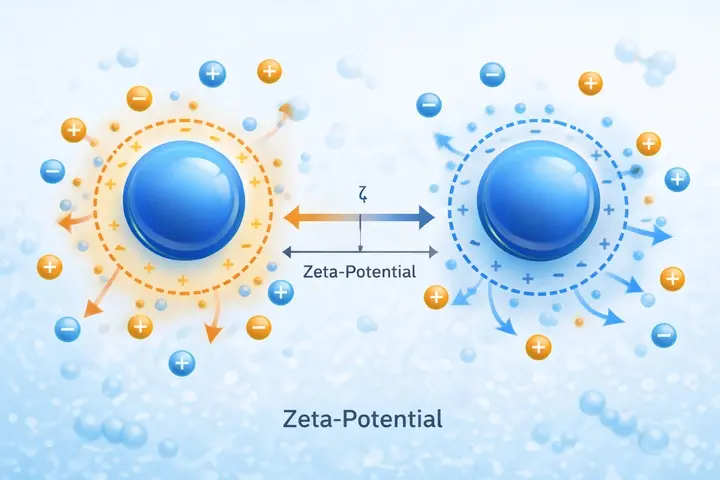
Messgröße für die elektrische Situation an der Grenzfläche eines Partikels in der Flüssigkeit. Es gilt als wichtiger Hinweis auf die Stabilität kolloidaler Systeme.
FAQ - Wissenswertes rund um Kolloide
Wer sich mit Kolloiden beschäftigt, möchte nicht nur Fachbegriffe lesen, sondern Zusammenhänge wirklich verstehen. In diesem FAQ-Bereich beantworten wir wichtige Fragen rund um Kolloide, Ionen, Stabilität und Partikelgrößen einfach und verständlich.
Ein Kolloid ist ein fein verteiltes System, bei dem sehr kleine Teilchen in einem anderen Medium, meist Wasser, verteilt sind, ohne sich vollständig darin zu lösen. Kolloide liegen damit zwischen einer echten Lösung und einer groben Suspension. Gerade in der Kolloidherstellung ist dieser Unterschied wichtig, weil die Eigenschaften stark von der Größe und Verteilung der Teilchen abhängen.
Ionen sind elektrisch geladene Atome oder Moleküle, die vollständig gelöst in einer Flüssigkeit vorliegen. Kolloide bestehen dagegen aus fein verteilten, nicht vollständig gelösten Partikeln. Dieser Unterschied ist für das Verständnis der Kolloidherstellung besonders wichtig, weil Ionen und kolloidale Partikel chemisch und physikalisch unterschiedlich reagieren.
Der Tyndall-Effekt beschreibt die Streuung von Licht an sehr feinen kolloidalen Teilchen. Dadurch kann ein Lichtstrahl in einer kolloidalen Flüssigkeit sichtbar werden. Der Tyndall-Effekt gilt als typisches Merkmal kolloidaler Systeme und hilft dabei, den Unterschied zwischen einem Kolloid und einer echten Lösung besser zu verstehen.
Agglomeration bedeutet, dass sich kleine Teilchen zu größeren Verbänden zusammenlagern. Bei Kolloiden ist das meist unerwünscht, weil die feine Verteilung der Partikel verloren gehen kann. Das kann die Stabilität, Gleichmäßigkeit und Qualität eines kolloidalen Systems beeinträchtigen.
Die Partikelgröße beeinflusst wichtige Eigenschaften eines Kolloids, zum Beispiel Stabilität, Lichtstreuung, Sedimentation und das optische Erscheinungsbild. Sehr feine Partikel bleiben oft besser verteilt als größere Teilchen. Deshalb ist die Partikelgröße ein zentraler Faktor bei der Kolloidherstellung und bei der Beurteilung der Qualität eines Kolloids.
Stabilität beschreibt, wie gut die feinen Teilchen über längere Zeit gleichmäßig in der Flüssigkeit verteilt bleiben. Ein stabiles Kolloid setzt sich nicht schnell ab und neigt weniger dazu, dass sich Teilchen zusammenlagern. Für die Kolloidherstellung ist eine gute Stabilität wichtig, weil sie wesentlich zur gleichbleibenden Qualität beiträgt.
Ein Kolloid erkennt man daran, dass sehr feine Teilchen in einer Flüssigkeit verteilt sind, ohne vollständig gelöst zu sein. Ein typisches Kennzeichen kann der Tyndall-Effekt sein, also die sichtbare Streuung eines Lichtstrahls in der Flüssigkeit. Auch Eigenschaften wie feine Verteilung, langsame Sedimentation und eine gleichmäßige Erscheinung spielen dabei eine Rolle.


